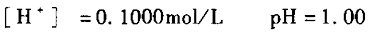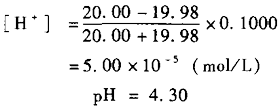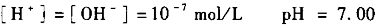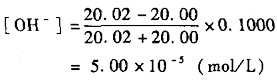现以NaOH液(0.1000mol/L)滴定20.00mlHCl液(0.1000mol/L)为例来讨论。设酸和碱的浓度分别为C
a、C
b,酸和碱的体积分别为V
a、V
b。
1.滴定开始前(V
b=0) 溶液的酸度等于盐酸的原始浓度,则
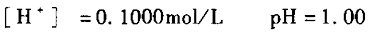
2.滴定开始至化学计量点前 随着NaOH的不断滴入,溶液中[H
+]逐渐减小,其大小取决于剩余HCl的量和溶液的体积。当滴入NaOH液19.98ml(化学计量点前0.1%)时,则
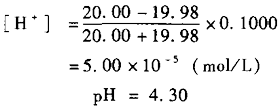
3.化学计量点(V
a= V
b) 时滴入NaOH液20.OOml,NaOH和HCl以等物质的量相互作用,溶液呈中性,则
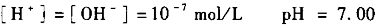
4.化学计量点后(V
a>V
b) 溶液的pH值由过量的NaOH的量和溶液的体积来决定。当滴入NaOH液20.02ml(化学计量点后0.1%)时,则
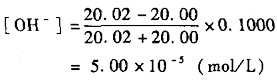
责任编辑:刀刀